Copy link
Mielomeningocele
Last updated: 04/01/2025
Puntos Clave
- El mielomeningocele se caracteriza por la herniación de los elementos durales y el tejido neural debido un defecto en la fusión del tubo neural durante el desarrollo embrionario.
- La falta de cierre de la placa neural expone el tejido a lesionarse por el trauma mecánico y químico contra la pared uterina y el líquido amniótico, respectivamente.
- El manejo quirúrgico postnatal sucede dentro de las primeras 72 horas para reducir el riesgo de infección. Se debe tener especial precaución en evitar mayor traumatismo o rotura del saco que recubre el defecto durante el manejo anestésico inicial del paciente.
Introducción y Epidemiologia
- El mielomeningocele es la anomalía congénita más común del sistema nervioso central.1
- La anomalía se caracteriza por la herniación del tejido neural y las meninges en un saco lleno de líquido cefalorraquídeo; si contiene solo meninges es conocido como meningocele y si contiene tejido neural y meninges se le llama mielomeningocele.2 (Figura 1)
- Resulta de un error en la fusión del tubo neural durante la tercera y cuarta semana del desarrollo embrionario,3 y tiene una incidencia establecida de 1-2 por cada mil nacidos vivos, siendo dicha incidencia mayor en niñas.4
- Los sobrevivientes tienen discapacidades que se correlacionan con el nivel de la lesión en la médula espinal. Las lesiones por encima de T4 se asocian con paraplejía.3
- En los pacientes reparados, la médula se puede anclar, lo que evita la migración cefálica del cono medular en la medida que el paciente crece lo cual se puede manifestar con disfunción vesical o intestinal, alteración sensorial y dolor lumbar.
- El cierre quirúrgico precoz es fundamental para evitar meningitis, ventriculitis y mejorar la función motora5 por lo que todo anestesiólogo deberá estar familiarizado con las consideraciones anestésicas para estos pacientes.
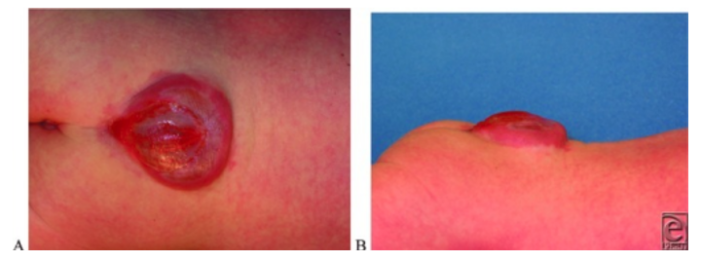
Figura 1. Mielomeningocele lumbosacro. Imagen A) posterior B) lateral (Fuente: Openi)
Fisiopatología
- El cierre incompleto del neuróporo caudal durante el periodo embrionario va a ocasionar la herniación y exposición del tejido neural y las meninges a líquido amniótico (Figura 2).6
- El mecanismo de la lesión a estas estructuras durante el desarrollo fetal se da por el roce mecánico del tejido neural contra la pared uterina y, además, una lesión química por exposición directa al ambiente de líquido amniótico en el saco gestacional.
- En la aparición de estas anomalías están implicados tanto factores genéticos como polimorfismos, así como la deficiencia de ácido fólico, uso de fármacos antiepilépticos, diabetes materna pregestacional y factores ambientales.7
- Estos factores pueden presentarse de forma aislada o como parte de varios síndromes genéticos o cromosomopatías. La mayoría son de etiología desconocida.8
- La mayoría de los defectos de la médula espinal son consecuencia del cierre anormal de los pliegues neurales y estas no sólo afectan el sistema nervioso central, sino también interfieren con la morfogénesis de los arcos vertebrales y la bóveda craneal, afectando por lo tanto meninges, vertebras, cráneo, músculos y piel.10
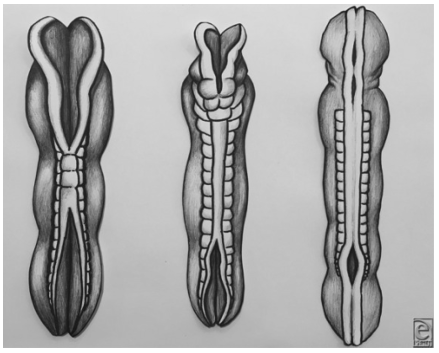
Figura 2. Cierre del tubo neural. El cierra se lleva a cabo en forma de zíper (cremallera) comenzando por el centro y luego extendiéndose craneal y caudal. La falla en el cierre del neuróporo caudal es lo que causa el mielomeningocele. (Fuente: Openi)
Presentación y Diagnóstico
Presentación Clínica
- El mielomeningocele puede aparecer a cualquier nivel a lo largo de la médula espinal, sin embargo, son más frecuentes en niveles torácicos bajos y lumbares1,10
- Entre más alta se encuentre la lesión, mayor el déficit sensitivo y motor del paciente.
- Las secuelas neurológicas asociadas para estos pacientes varían desde la parálisis total o parcial de miembros inferiores, pérdida de sensibilidad en extremidades, pérdida en el control de esfínteres, defectos encefálicos y ortopédicos.11
- El mielomeningocele se presenta con hidrocefalia asociada a malformación de Arnold Chiari en 80-90% de los pacientes (Figura 5). Por esta razón, es frecuente que estos pacientes requieran la colocación de una derivación ventrículo-peritoneal en algún momento en la evolución de su tratamiento.1,9
- También puede asociarse a otras malformaciones como pie equinovaro, subluxación de cadera, alteraciones del aprendizaje e hidroanencefalia.12,13
Diagnóstico
- El ultrasonido y la cuantificación de Ժ-feto proteína materna desde el primer trimestre permiten el screening prenatal14 (Figura 3).
- La cuantificación de proteína ácida fibrilar glial (PAFG) de los astrocitos aumenta su concentración en líquido amniótico relacionado a la gravedad de la neurodegeneración asociada al mielomeningocele, siendo esta una estrategia actual de detección.15
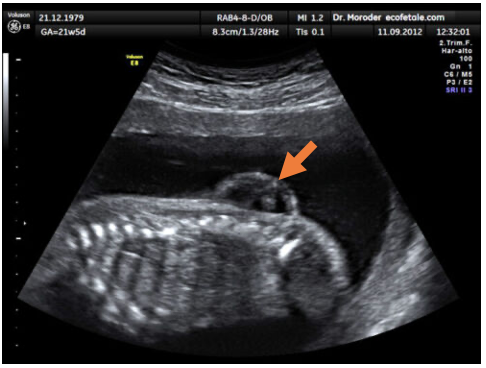
Figura 3. Mielomeningocele lumbar en un feto de 21 semanas de gestación (Fuente: Wolfgang Moroder, Wikimedia. CC BY SA 3.0)
Tratamiento
- El cierre quirúrgico del defecto puede realizarse mediante reparación prenatal por histerotomía
- La cirugía fetal ha demostrado que si se realiza antes de las 26 semanas disminuye el riesgo de muerte, necesidad de derivación a los 12 meses y mejoras en la función motora y mental a los 30 meses
- La intervención fetal se asocia con tasas más altas de parto prematuro y mayor morbilidad materna.16
- La cirugía posnatal debe realizarse de forma temprana, dentro de las 72 horas después del nacimiento para reducir el riesgo de infecciones. Esta tiene como objetivos terapéuticos:
1. Cubrir el cordón medular expuesto.
2. Liberar la placa neural de la piel anormal circundante y reposicionar dentro del saco dural.
3. Reconstruir la duramadre para prevenir fuga de LCR, infección y reinserción de la médula espinal14,15 (Figura 4).
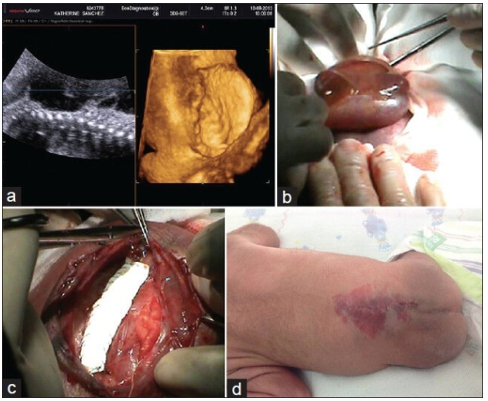
Figura 4. Reparación Quirúrgica de Mielomeningocele. División de Neurocirugía. Hospital Universitario Japonés. Santa Cruz de la Sierra. Bolivia. (Fuente: Openi)
Consideraciones Anestésicas
Evaluación Preoperatoria
- Deberán conocerse los antecedentes de la madre, la historia prenatal, historia del nacimiento y antecedente de prematuridad.12,13
- Se deberá evaluar la función neurológica y descartar la presencia de una malformación de Arnold Chiari tipo II, previo a la intervención (Figura 5).
- Descartar cardiopatías u otras anomalías congénitas asociadas.13
- Anticipar la posibilidad de una vía aérea difícil debido a la dificultad para posicionar el paciente durante la inducción.
- Tomar en cuenta la posibilidad de sensibilización temprana al látex en estos pacientes por exposición repetida a través de catéteres endovenosos, sonda vesical, etc.9,15
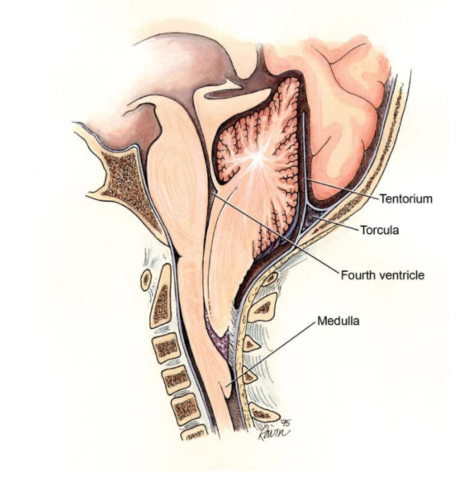
Figura 5. Malformación Chiari Tipo II (Wikimedia Commons. CC BY 2.0)
Manejo Intraoperatorio
- La técnica anestésica de elección es la anestesia general endotraqueal.13
- Previo a la inducción se recomienda proteger el defecto, ya sea con un rodete o una almohadilla de gel (en forma de dona), para evitar que este se comprima o se rompa.
- Cuando el defecto es muy extenso se sugiere posicionar al paciente en decúbito lateral durante la inducción e intubación endotraqueal.8,9,12
- La inducción anestésica puede realizarse por vía endovenosa o inhalatoria,
- El sevoflurano es preferible por su rápido inicio de acción y baja pungencia.15
- El Propofol y los opioides como adyuvantes permiten realizar una inducción endovenosa segura con la precaución de evitar episodios de hipotensión que se asocia con isquemia cerebral.9
- La intubación sobre una almohadilla o en decúbito lateral puede ser dificultosa por lo que se recomienda la disponibilidad del fibroscopio flexible y/o videolaringoscopio.8
- La intubación nasotraqueal permite un buen margen de seguridad en el tubo endotraqueal con el paciente en posición prono para el abordaje quirúrgico.
- Se puede utilizar relajación muscular para favorecer la intubación. El rocuronio es seguro y se utiliza con frecuencia.9,12
- La pérdida sanguínea estimada a este procedimiento generalmente no requiere de transfusión.
- Cuando el defecto es extenso incrementa el riesgo de sangrado, y en dichos casos se sugiere considerar el uso de un catéter arterial y accesos venosos múltiples (al menos dos vías periféricas funcionales).11
- Usualmente se coloca sonda vesical en estos pacientes, que se suele mantener hasta el postoperatorio.
- Mantener la normotermia es fundamental en esta población.12
Cuidados Postoperatorios
- Dado que la mayoría son neonatos, se recomienda sean trasladados a cuidados neonatales en el posoperatorio.
Preguntas
Responde preguntas aquí.
References
- Naseri Alavi SA, Fluss R, Lehner K, et al. Tethered cord prevalence among patients with prenatal or postnatal myelomeningocele repair. Childs Nerv Syst. 2024;40(11):3621-3628. doi:10.1007/s00381-024-06584-5 PubMed
- Cali-Tobar L, Lautaro Chávez-Iza, López-Mayorga A. Diagnóstico, manejo y tratamiento actual del mielomeningocele fetal. Revista de la Facultad de Ciencias Médicas Quito, año 2022, vol. 47(2). Link
- Gomes JRB. Mielomeningocele. En: Gallas A. Rehabilitación, teoría y práctica. Lestu Publishing Company. Published online June 27, 2022:309-337.3/cap.22. Link
- Fonseca F, Ortega J, Mielomeningocele: actualización para la práctica clínica. Revista Médica Hondureña. Año 2021. Vol. 89, pág. 35-37. Link
- Kowitzke B, Cohrs G, Leuschner I, et al. Cellular Profiles and Molecular Mediators of Lesion Cascades in the Placode in Human Open Spinal Neural Tube Defects. J Neuropathol Exp Neurol. 2016;75(9):827-842. doi:10.1093/jnen/nlw057 PubMed
- Heuer GG, Moldenhauer JS, Scott Adzick N. Prenatal surgery for myelomeningocele: review of the literature and future directions. Childs Nerv Syst. 2017;33(7):1149-1155. doi:10.1007/s00381-017-3440-z PubMed
- Lara, Arruza Gómez, L, Villar V, Ortiz A. Defectos del tubo neural: Epidemiología y factores perinatales asociados en fetos y recién nacidos. Acta Pediátrica Española. 2025;66(9):445-451. Link
- Pardo R, Suazo J, Castillo S, et al. Estudio de asociación de base familiar entre polimorfismos de MTHFR y mielomeningocele en Chile. Revista médica de Chile. 2014;142(5):587-592. Link
- Dewan MC, Wellons JC. Fetal surgery for spina bifida. J Neurosurg Pediatr. 2019;24(2):105-114. doi:10.3171/2019.4.PEDS18383 PubMed
- Tung C, Vutskits L, G. Soriano, Congenital Neurosurgical Lesions. In: Essentials of pediatric neuroanesthesia, Soriano McClain: Cambridge University Press, 2019:77-84
- McClain CD, Soriano SG. The central nervous system: pediatric neuroanesthesia. In: Holzman RS, Mancuso TJ, Polaner DM, eds. A Practical Approach to Pediatric Anesthesia, 2nd ed. Philadelphia: Wolters Kluwer; 2016:226–64.
- Viscomi CM, Abajian JC, Wald SL, Rathmell JP, Wilson JT. Spinal anesthesia for repair of meningomyelocele in neonates. Anesth Analg. 1995;81(3):492-495. doi:10.1097/00000539-199509000-00011 PubMed
- Jagannathan N, Sohn L, Fiadjoe JE. Paediatric difficult airway management: what every anaesthetist should know!. Br J Anaesth. 2016;117 Suppl 1:i3-i5. doi:10.1093/bja/aew054 PubMed
- Kim AG, Danzer E, Moldenhauer JS, et al. Amniotic Fluid Concentrations of Glial Fibrillary Acidic Protein Do Not Correlate with Prenatal Metrics in Fetuses with Myelomeningocele. Fetal Diagn Ther. 2018;43(4):297-303. doi:10.1159/000478258 PubMed
- Holzman RS. Clinical management of latex-allergic children. Anesth Analg. 1997;85(3):529-533. doi:10.1097/00000539-199709000-00009 PubMed
- Adzick NS, Thom EA, Spong CY, et al. A randomized trial of prenatal versus postnatal repair of myelomeningocele. N Engl J Med. 2011;364(11):993-1004. doi:10.1056/NEJMoa1014379 PubMed
Other References
- Chatterjee D. Myelomeningocele. OpenAnesthesia. Published January 2018. Updated January 2023 Accessed March 6, 2023. Link
Copyright Information

This work is licensed under a Creative Commons Attribution-NonCommercial-NoDerivatives 4.0 International License.